


Klar ist dabei, dass die Einnahme täglich erfolgen muss, um die volle Wirksamkeit zu erhalten. Es wird insbesondere
in Studien in der 3. Welt intensiv diskutiert, dass eine oder zwei wöchentliche Einnahmen genauso effektiv wären wie
die tägliche. Dies ist nach Versuchen mit 59Fe-Präparten eindeutig widerlegt und entspricht auch nicht der Erfahrung
mit Patienten mit Eisenmangelanämie. Die tägliche und nüchterne Einnahme von oralem Eisen ist effektiver als
einmal wöchentlich und/oder mit der Mahlzeit (23,24).
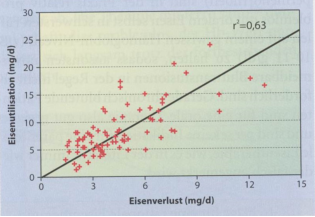
Abb. 4. Korrelation zwischen Eisenutilisation und Eisenverlust bei 82 Patienten mit Hypermenorrhoe oder
gastrointestinalem Blutverlust unter oraler Eisentherapie mit 1x100 mg Fe(II)/Tag (Eryfer® oder ferro sanol®
duodenal, nüchtern). Je höher der Blutverlust bei Patienten, desto mehr Eisen wird offenbar absorbiert und für die
Erythropoese zur Verfügung gestellt.
Nebenwirkungen einer oralen Eisentherapie
Unverträglichkeiten, adverse Reaktionen auf eine orale Eisentherapie stellen ein übertriebenes und gleichzeitig ein
in Vergessenheit geratenes Thema dar. Übertrieben in so fern, als das eine angebliche geringe orale Intoleranz
aktuell immer wieder als Begründung herhalten muss für die Notwendigkeit einer parenteralen Eisentherapie mit neu
entwickelten, meist teuren Eisenpräparaten. In Vergessenheit geraten deshalb, weil unsere wissenschaftlichen
Erkenntnisse ganz überwiegend aus Studien vor 1975 stammen; seither gibt es nur wenige neue Publikationen.
Als Grundlage des Wissens über Nebenwirkungen einer oralen Eisentherapie gelten umfangreiche Studien von
Hallberg und Sölvell aus den 60iger und 70ger-Jahren des letzten Jahrhunderts an über 2000 Personen (26, 2). In
verschiedenen Testserien wurde Eisensulfat als Referenzstandard verwendet. Die tägliche Dosis war mit entweder 3
x 60 mg Fe/Tag oder 3 x 75 mg/Tag relativ hoch.
Nebenwirkungen werden durch eine hohe Konzentration von ionischem Eisen (Fe2+) im Darm hervorgerufen
(Tabelle 6.4) und sind deshalb meistens gastrointestinaler Art, wie z.B. Übelkeit, Sodbrennen, Verstopfung,
Durchfall. Der Absorptionsvorgang muss eine wichtige Rolle daran spielen, denn nicht-bioverfügbare Eisenpräparate
zeigen eine sehr geringe Nebenwirkungsrate. Die Untersuchung von Eisenpräparaten sollte deshalb in Studien
erfolgen, die gleichzeitig die Bioverfügbarkeit und die Nebenwirkungen untersuchen. Wegen der Häufigkeit von
unspezifischen Beschwerden in Medikamentenstudien ist dabei unabdingbar, dass das Studiendesign einen
Placeboarm vorsieht, wünschenswert wäre auch eine positiv-Kontrolle in Form eines bekannten Eisenpräparates (2).
Nebenwirkungen einer oralen Eisentherapie
•
abhängig von der Wirksamkeit (=Absorption) des jeweiligen Präparates
•
abhängig von der Einzel- und Tagesdosis (signifikant ab >= 100 mg Fe/Tag)
•
Zusätze wie Vitamin C verstärken die Häufigkeit
Einzelne Symptome:
•
Verstopfung
•
Durchfall
•
Sodbrennen
•
Übelkeit
•
Epigastrische Schmerzen, Krämpfe
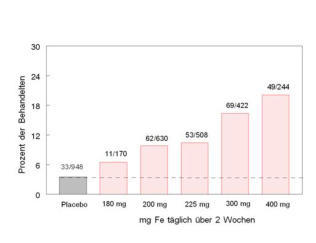
Nach Placeboeinnahme gaben 12.4-13.9 % der Probanden gastrointestinale Nebenwirkungen an. Eine
Eisentherapie oberhalb von 100 mg Fe/Tag erzeugten häufigere Beschwerden (20-30 % der Fälle) als Placebo. Ein
Beispiel mit den Symptomen Übelkeit und epigastrische Schmerzen zeigt Abb. 5.
Abb. 5. Häufigkeit der Symptome Übelkeit und epigastrische Schmerzen nach zunehmenden Dosen von
Eisen(II)-Sulfat-Tabletten über 2 Wochen (nach Hallberg et al. Lit. 26)
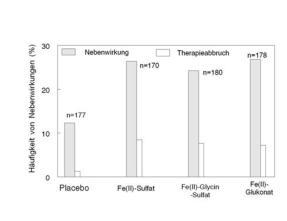
Es gab keine signifikanten Unterschiede zwischen verschiedenen Eisenverbindungen wie Eisen(II)-Sulfat-, -
Fumarat, - Glukonat,-, Eisen(II)-Glycin-Sulfat, Eisen(II)-Sulfat plus Bernsteinsäure, Eisen(II)-Succinat (Abb. 6.5). Bis
zu 10 % der Personen brachen die Therapie über 2 Wochen ab.
Abb. 6. Häufigkeit von Nebenwirkungen nach Gabe von verschiedenen Eisenverbindungen. Dosis jeweils 3 x 60 mg
Fe/Tag (nach 26)
Vitamin C, als Zusatz zu Eisenpräparaten, steigerte in einer kleinen Serie aus 30 Probanden die Häufigkeit von
angegebenen Nebenwirkungen (27). Ähnlich wirkten auch andere Zusätze wie Sorbitol, Mannitol oder Xylose, die als
Stimulatoren der Absorption ausprobiert wurden.
Es wurden verschiedene Versuche unternommen, die Inzidenz von Nebenwirkungen dadurch zu verringern, dass
„slow-release“-Präparate konzipiert wurden, die jeweils nur langsam Eisen freisetzen.
Es kann postuliert werden, dass wenn Eisen aus einem Präparat nicht freigesetzt wird, bevor es den Magen passiert
hat, es zu weniger Nebenwirkungen kommt. Allerdings gefährdet diese verzögerte Wirkstofffreisetzung eine
möglichst hohe Bioverfügbarkeit. Einige solcher Präparate sind nur offenbar sehr schlecht wirksam (28). Andere
scheinen bei akzeptabler Wirksamkeit auch eine bessere Verträglichkeit zu haben. Insbesondere für diese
aufwendigen Eisenpräparate ist der individuelle Nachweis einer verbesserten Verträglich bei gleichzeitig gegebenen
hohen Wirksamkeit unbedingt erforderlich. Am Bespiel des Eisen(III)-Hydroxy-Polymaltose-Komplexes kann man in
der Literatur viele Aussagen über eine optimale Verträglichkeit finden, während kritische Studien diesem Präparat bis
heute unwiderlegt eine praktisch nicht-vorhandene Bioverfügbarkeit bescheinigen.
Neuere, detaillierte Studien über die Toleranz von oralen Eisenpräparaten im Vergleich sind eher Mangelware. Hier
gibt es meist nur Angaben zu einzelnen neuen Präparaten. In einer Studie aus dem Jahr 1993 wurden z.B. 549
Patienten mit Eisenmangel 60 Tage mit einem Präparat Eisen-Protein-Succinate-Komplex behandelt (Dosis 2x 60
mg/Tag) und mit einer Kontrollgruppe aus 546 Patienten, die mit einer kommerziellen Medikation von „controlled-
release“ Eisen(II)-Sulfat (1x 105 mg) behandelt wurde, verglichen. Bei gleicher Wirksamkeit gaben 63 Patienten
(11.5%) aus der untersuchten Gruppe 69 adverse Reaktionen an (25 mal Sodbrennen, 19 Verstopfung, 25
abdominale Schmerzen) gegenüber 141 Ereignissen in der Kontrollgruppe bei 127 Patienten (26.3%) (33 mal
Sodbrennen, 31 epigastrische Schmerzen, 23 Verstopfung, 32 abdominale Schmerzen, 8 Hautausschläge, 14
Übelkeit). (29). Bei dieser Studie fällt die Häufigkeit von Nebenwirkung in der Kontrollgruppe untypisch hoch für
Eisen(II)-Sulfat bei dieser Dosierung auf, während die Häufigkeit in der verum-Gruppe der Placeborate entspricht.
Eine andere Art von aktuellen Studien zu Nebenwirkungen von oraler Eisentherapie ist der Vergleich mit einem
parenteralen Eisenpräparat. In diesen Studien soll die bessere Verträglichkeit der jeweiligen i.v. Gabe nachweisen
werden, was meist problemlos gelingt, weil hierbei keine gastrointestinalen Nebenwirkungen zu erwarten sind. Ein
Beispiel ist eine Studie von Schröder et al. in der 46 Patienten mit Eisenmangelanämie entweder Eisen-Sucrose i.v.
über 5 Wochen oder oral Eisen(II)-Sulfat (100-200 mg Fe/Tag) über 6 Wochen erhielten. Bei ansonsten gleicher
Wirksamkeit (Hb-Anstieg) brachen 5 Patienten (20.8 %) die orale Eisentherapie ab, während nur 1 Patient (4.5 %)
aus der i.v.-Gruppe wegen Nebenwirkungen nicht weiterbehandelt wurde (30). Auch hier stellt sich die Frage nach
einer ungewöhnlich hohen Zahl von Nebenwirkungen in dem oralen Arm.
Zusammenfassung
Eine orale Eisentherapie führt nicht außergewöhnlich häufig zu Unverträglichkeitsreaktionen. Eine normal dosierte
Eisentherapie von 100 mg Fe(II)Tag dürfte bei den meisten Eisenpräparaten im Rahmen der Placebo-
Nebenwirkungsrate von 12-14 % liegen.
Nach unserer Erfahrung ist die Aufklärung des Patienten über Sinn und Dauer einer Eisentherapie besonders
wichtig, um die Akzeptanz der Therapie zu erhöhen. Hilfreich dabei die Information, dass Eisen kein übliches
Medikament ist, sondern ein essentielles Spurenelement, das dem Patienten bei Eisenmangel fehlt. Häufig sind
Reaktionen wie Verstopfung oder Durchfall auch transienter Art, weil sich die Darmbakterien auf die hohe
Eisendosierung im Dickdarm einstellen müssen.
Wege, um eine adverse Effekte einer Eisentherapie zu minimieren
•
Aufklärung über den Sinn und notwendige Dauer einer Eisentherapie
•
keine unnötig hohen Dosis (Tagesdosis meist 100 mg Fe/Tag ausreichend)
•
Einnahmezeitpunkt vor dem Mittagessen oder vor dem Abendessen
•
Tagesdosis in mehrere Portionen auf den Tag verteilen
•
Wechsel zu anderem Eisenpräparat
•
Einnahme zusammen mit der Mahlzeit (setzt die Wirksamkeit um 40-60 % herab!)
Literatur Eisentherapie
1.
Beutler E. History of Iron in Medicine. Blood Cells, Molecules, and Diseases 2002; 29(3): 297–308
2.
Hallberg L. Oral iron therapy-factors affecting the absorption. In Hallberg L, Harwerth HG, Vannotti A (eds): Iron deficiency.
Pathogenesis, Clinical Aspects, Therapy. London , Academic Press, 1970, pp. 551-72
3.
Heinrich HC. Bioverfügbarkeit und therapeutische Wirksamkeit oraler Eisen(II)- und Eisen(III)präparate. Schweiz.
Apotheker-Zeitung 1986; 22:1231-1256
4.
Muir A, Hopfer U. Regional specificity of iron uptake by small intestinal brush-border membranes from normal and iron-
deficient mice. Am J Physiol Gastrointest Liver Physiol 1985; 248: G376-G379
5.
F. Canonne-Hergaux, S. Gruenheid, P. Ponka, et al. Cellular and Subcellular Localization of the Nramp2 Iron Transporter in
the Intestinal Brush Border and Regulation by Dietary Iron. Blood 1999; 93(12): 4406 - 17
6.
Nielsen P, Kongi R, Zimmermann I, Gabbe EE. Bioverfügbarkeit von oralen Eisenpräparaten. In-vitro-Freisetzung von
Eisen als einfaches und schnelles Prüfverfahren. Teil I: Der Allgemeinarzt 1997; 6:524-527, 621-626
7.
Fairweather-Tait S, Phillips I, Wortley G, Harvey L, Glahn R. The use of solubility, dialyzability, and Caco-2 cell methods to
predict iron bioavailability. Int J Vitam Nutr Res. 2007; 77(3):158-65
8.
Wienk KJH, Marx JJM, Beynen AC. The concept of iron bioavailability and its assessment Eur J Nutr 1999; 38: 51–75
9.
Brise H, Hallberg L. Absorbability of different iron compounds. Acta med Scand Suppl 1962; 376:23-37
10.
Lehmann W D, Fischer. R and Heinrich HC. Iron absorption in man calculated from erythrocyte incorporation of the stable
isotope iron-54 determined by fast atom bombardment mass spectrometry. Anal Biochem 1988; 172: 151–159
11.
Whittaker PG, Barrett JFR, Lind T. The erythrocyte incorporation of absorbed non-haem iron in pregnant women. Brit J Nut
2001; 86, 323–329
12.
Dietzfelbinger H. Bioavailability of bi- and trivalent oral iron preparations. Investigations of iron absorption by
postabsorption serum iron concentrations curves. Arzneim-Forsch/Drug Res 1987; 37:107-12
13.
Heinrich HC, Fischer R. Correlation of Postabsorptive Serum Iron Increase and Erythrocyte-59Fe-Incorporation with the
Whole Body Retention of Absorbed 59Fe. Klin Wochenschr 1982;60:1493-4496
14.
Hoppe M, Hulthén L, Hallberg L. Serum iron concentration as a tool to measure relative iron absorption from elemental iron
powders in man. Scand J Clin Lab Invest. 2003;63(7-8):489-96
15.
Nielsen P, Kongi R, Buggisch P, Fischer R. Bioavailability of oral iron drugs as judged by a 59Fe-whole-body counting
technique in patients with iron deficiency anaemia. Therapeutic efficacy of iron(II)-glycine sulfate. Arzneim.Forsch/Drug
Res 2005; 55:376-381
16.
Heinrich HC. Bioavailability of trivalent iron in oral iron preparations. Therapeutic efficacy and iron absorption from simple
ferric compounds and high- or low-molecular weight ferric hydroxide-carbohydrate complexes. Arzneim-Forsch/Drug Res
1975; 25: 420-6
17.
Heinrich HC, Fischer R, Gabbe EE, Theobald N. Bioverfügbarkeit des in einem oralen Eisenpräparat enthaltenen
Eisen(III)hyroxid-Dextran-Komplexes. Klein Wochenschr 1983; 61:103-110
18.
Nielsen P, Gabbe EE, Fischer R, et al. Bioavailability of iron from oral ferric polymaltose in humans. Arzneim-Forsch/Drug
Res 1994; 44: 743-8
19.
Hershko C, Ianculovich M, Souroujon M. Decreased Treatment Failure Rates following Duodenal Release Ferrous Glycine
Sulfate in Iron Deficiency Anemia Associated with Autoimmune Gastritis and Helicobacter pylori Gastritis. Acta Haematol
2007;118:19-26
20.
Kaltwasser JP, Werner E, Niechzial M. Bioavailability and therapeutic efficacy of bivalent and trivalent iron
preparations.Arzneim Forsch 37: 122–129
21.
Mehta BC. Mehta BC . Failure of oral iron therapy in treatment of iron deficiency anemia: Pharmaceutical iatrogenic
cause. Indian J Med Sci 2001;55:157-8
22.
Toblli JE, Brignoli R. Iron(III)-hydroxide polymaltose complex in iron deficiency anemia / review and meta-analysis.
Arzneimittelforschung. 2007;57(6A):431-8
23.
Faqih AM, Kakish SB, Izzat M. Effectiveness of intermittent iron treatment of two- to six-year-old Jordanian children with
iron-deficiency anemia. Food Nutr Bull. 2006;27(3):220-7
24.
Cook JD, Reddy MB. Efficacy of weekly compared with daily iron supplementation. Am J Clin Nutr 1996; 62:117–20
25.
Hallberg l. Combating iron deficiency: daily administration of iron is far superior to weekly administration. Am J Clin Nutr
1998;68:213–7
26.
Hallberg L, Ryttinger L, Sölvell L. Side-effects of oral iron therapy. A double-blind study of different iron compounds in
tablet form. Acta Med Scand Suppl 1966; 459: 3 –10
27.
Hallberg L, Sölvell L, Brise H. Search for substances promoting the absorption of iron.Sudies on absorption and side
effects. Acta Med Scand Suppl 1966; 459: 11-21
28.
Rudinskas L, Paton TW, Walker SE, Dotten DA, Cowan DH. Poor clincal response to enteric-coated iron preparations.
CMAJ 1989;141:565-566
29.
Liguori L. Iron protein succinylate in the treatment of iron deficiency: controlled, double-blind, multicenter clinical trial on
over 1,000 patients. Int J Clin Pharmacol Ther Toxicol 1993; 31(3):103-23




















© www.eiseninfo.de
Orale Eisentherapie 3
Empfehlungen für eine bedarfsangepasste Therapie
Bei Eisenmangel mit und ohne Anämie wird als Therapie
der Wahl uneingeschränkt die orale Eisentherapie
empfohlen. Es sollten nur Präparate verwendet werden,
deren Wirksamkeit man gut von Therapie bei früheren
Patienten kennt bzw. die ihre Qualität in unabhängigen
Studien nachgewiesen haben.
Was in der Literatur wenig bekannt ist, wie gut die
Bioverfügbarkeit einer Eisentherapie durch die vorhandene
Blutverluste eingestellt werden kann (Abb. 6.4). Je höher
der Bedarf an Eisen für die Blutneubildung ist, desto mehr
Eisen wird aus einer effektiven Eisentherapie absorbiert.
Dadurch reguliert sich die orale Eisentherapie in gewissen
Grenzen selbstständig.
Therapie
Bei Eisenmangel mit und ohne Anämie wird als Therapie
der Wahl uneingeschränkt die orale Eisentherapie
empfohlen. Es sollten nur Präparate verwendet werden,
deren Wirksamkeit man gut von Therapie bei früheren
Patienten kennt bzw. die ihre Qualität in unabhängigen
Studien nachgewiesen haben.
Was in der Literatur wenig bekannt ist, wie gut die
Bioverfügbarkeit einer Eisentherapie durch die vorhandene
Blutverluste eingestellt werden kann (Abb. 6.4). Je höher
der Bedarf an Eisen für die Blutneubildung ist, desto mehr
Eisen wird aus einer effektiven Eisentherapie absorbiert.
Dadurch reguliert sich die orale Eisentherapie in gewissen
Grenzen selbstständig.
 Therapie
Bei Eisenmangel mit und ohne Anämie wird als Therapie
der Wahl uneingeschränkt die orale Eisentherapie
empfohlen. Es sollten nur Präparate verwendet werden,
deren Wirksamkeit man gut von Therapie bei früheren
Patienten kennt bzw. die ihre Qualität in unabhängigen
Studien nachgewiesen haben.
Was in der Literatur wenig bekannt ist, wie gut die
Bioverfügbarkeit einer Eisentherapie durch die vorhandene
Blutverluste eingestellt werden kann (Abb. 6.4). Je höher
der Bedarf an Eisen für die Blutneubildung ist, desto mehr
Eisen wird aus einer effektiven Eisentherapie absorbiert.
Dadurch reguliert sich die orale Eisentherapie in gewissen
Grenzen selbstständig.
Therapie
Bei Eisenmangel mit und ohne Anämie wird als Therapie
der Wahl uneingeschränkt die orale Eisentherapie
empfohlen. Es sollten nur Präparate verwendet werden,
deren Wirksamkeit man gut von Therapie bei früheren
Patienten kennt bzw. die ihre Qualität in unabhängigen
Studien nachgewiesen haben.
Was in der Literatur wenig bekannt ist, wie gut die
Bioverfügbarkeit einer Eisentherapie durch die vorhandene
Blutverluste eingestellt werden kann (Abb. 6.4). Je höher
der Bedarf an Eisen für die Blutneubildung ist, desto mehr
Eisen wird aus einer effektiven Eisentherapie absorbiert.
Dadurch reguliert sich die orale Eisentherapie in gewissen
Grenzen selbstständig.

























