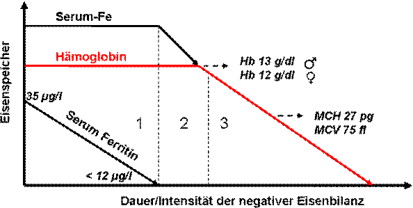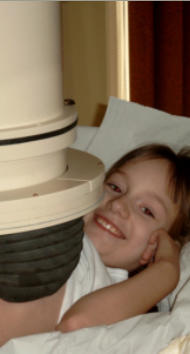


Abb. 1. Diagnostische Parameter bei Eisenmangel mit und ohne Anämie nach Hausmann und Heinrich. 1,
prälatenter Eisenmangel; 2. latenter Eisenmangel; 3. manifester Eisenmangel. Mit den Parametern Hämoglobin,
Serum-Ferritin, Serum-Eisen und Transferrin kann man den typischen Eisenmangelpatienten ausreichend genau
beschreiben.
Sind die Eisenspeicher erschöpft, so wird in einer weiteren Stufe der relativ kleine Transporteisenpool
beeinträchtigt (latenter Eisenmangel). Dies kann an Patienten mit normaler Hämoglobinkonzentration an
den erniedrigten Werten für Serum-Eisen und Transferrin-Eisen-Sättigung, sowie am erhöhten Transferrin,
erkannt werden. Hier hat sich jetzt der Stoffwechsel auf Eisenmangel eingestellt, die Transferrinsynthese
in der Leber wird hochgefahren, um vermehrt Eisen in Zellen zu transportieren. 
Verstärkt sich der Eisenmangel weiter (manifester Eisenmangel), sinkt der Hb-Wert von neugebildeten
Erythrozyten unterhalb der Norm ab. Bei einer Lebensdauer von 120 Tage für normale geformte
Erythrozyten, sinken der mittlere Hämoglobingehalt und das mittlere Erythrozytenvolumen erst langsam
ab. Eine mikrozytäre und hypochrome Anämie spricht also für einen länger bestehenden schweren
Eisenmangel, im Unterschied zu einer normozytären, normochromen Blutungsanämie.
Mit den hier erwähnten einfachen Blutparametern kann man am Patienten diese drei Schweregrade des
Eisenmangels gut auseinander halten. Im Falle einer Therapie mit ausreichenden Eisenmengen
normalisieren sich diese Parameter in umgekehrter Reihenfolge, d.h. das Hämoglobin reagiert zuerst, das
Serum-Ferritin wird erst am Ende nach einiger Zeit wieder ansteigen. 
Absoluter und Funktioneller Eisenmangel
Der Begriff funktioneller Eisenmangel wurde geprägt im Zusammenhang mit der Behandlung von
Patienten mit renaler Anämie mit rekombininanten humanen Erythropoetin (r-HuEpo) (2, 3). Die Therapie
mit r-HuEPO ist oft deutlich wirksamer, wenn gleichzeitig mit i.v. Eisen behandelt wird und zwar nicht nur
bei Patienten mit niedrigem Serum-Ferritin, die keine Eisenreserven haben und damit einen absoluten
Eisenmangel aufweisen. Eisentherapie ist auch wirksam bei Patienten mit normalen, oder sogar erhöhten
Serum-Ferritin-Werten. Ein funktioneller Eisenmangel besteht also, wenn zwar die Eisenspeicher
ausreichend mit Eisen gefüllt sind, es aber trotzdem zu einer unzureichenden Eisenversorgung der durch
EPO angetriebenen Erythropoese kommt. In diesen Fällen ist das Serum-Ferritin offensichtlich ein
schlechter Parameter, um die Veränderung der Eisenspeicher zuverlässig anzuzeigen (4). Eine adäquate
Eisenversorgung lässt sich durch Messung des retikulozytären Hämoglobingehalts (Chr) und durch die
Bestimmung des Prozentsatzes an hypochromen Erythrozyten (HYPO) sensitiver und spezifischer
ermitteln. 
Ein funktioneller Eisenmangel tritt auch bei normalen Personen auf, die mehrmals in kurzer Zeit
Blutspenden und dabei mit r-HuEPO behandelt wurden (5). Ein gleicher Effekt dürfte auch bei Sportlern
unter Höhentrainingsbedingungen (legal) bzw. Doping mit r-HuEPO (illegal) (6). Auch im Zusammenhang
mit übergewichtigen Patienten wird der Begriff des funktionellen Eisenmangels bereits benutzt (7). In
allen diesen Fällen erhöht die begleitende Eisentherapie die Wirksamkeit und senkt die Kosten für die
Erythropoetinbehandlung. 
Ein funktioneller Eisenmangel findet sich darüber hinaus auch bei chronisch entzündlichen oder malignen
Erkrankungen, bei denen Eisen aus der Zirkulation zurück in die Speicher verlagert wird. Es liegt nahe,
dass das Eisen-Hormon Hepcidin an der Regulation der Eisenverteilung bei Patienten mit renaler Anämie
beteiligt ist und es hat bereits Untersuchungen zu diesem Thema gegeben, wobei die Ergebnisse bisher
sehr variabel sind (8). 
Speichereisenmangel, eisendefizitäre Erythropoese, Eisenmangelanämie
Einer Arbeit des Autor J. Hastkas folgend wurde in den aktuellen Leitlinien der Deutschen Gesellschaft für
Hämatologie und Onkologie die Begriffe funktioneller Eisenmangel und eisendefizitäre Erythropoese aus
dem Bereich der Patienten mit renaler Anämie jetzt auf alle Patienten übertragen (Abb. 2) (9,10). 
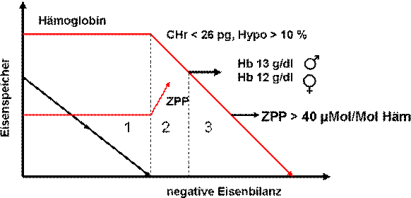
Abb. 2. Einteilung des Schweregrads und diagnostische Parameter von Eisenmangel nach Hastka et al. für die
Deutsche Gesellschaft für Hämatologie/Onkologie (www.dgho.de). 1.) Speichereisenmangel, 2.) eisendefizitäre
Erythropoese (=“funktioneller Eisenmangel“), 3. Eisenmangelanämie. ZPP und Chr zeigen empfindlich die
Eisendefizitäre Erythropoese an.
Das Stadium 1 (Speichereisenmangel) ist gleichzusetzen mit dem prälatenten Eisenmangel nach
Hausmann und Heinrich. Der wesentliche Unterschied liegt in dem Begriff „eisendefizitären Erythropoese“
(Stadium 2), der hier auch als funktioneller Eisenmangel bezeichnet wird. Bei der eisendefizitären
Erythropoese wird der Eisenmangel zur Erkrankung, indem die Zellen nicht mehr ausreichend mit Eisen
versorgt werden können. Einzelne Erythrozyten werden bereits hypochrom und mikrozytär, was im
peripheren Blutbild noch nicht zu erkenne ist. Im Stadium 3 (Eisenmangelanämie) ist die mangelhafte
Eisenversorgung der Körperzellen bereits so ausgeprägt, dass die Hämoglobinnormwerte unterschritten
werden. Zwischen Stadium 2 und 3 ist also nur noch ein gradueller Unterschied, was die Bedeutung des
Stadium 2 noch mehr betont. 
Bei diesem Konzept ist der Begriff des funktionellen Eisenmangels irreführend und sollte nicht verwendet
werden, da dieser Begriff bei Patienten mit renaler Anämie eingeführt ist und dort eindeutig eine andere
Bedeutung hat. Wenn hier funktioneller Eisenmangel als Einschränkung von physiologischen Funktionen
durch den Mangel an Eisen gemeint ist, dann ist auch dies unpräzise, denn es gibt klinische Symptome
wie Müdigkeit und kognitive Leistungsverminderungen bereits früher im Stadium des Speichermangels.
Als letztes Konzept wird im Folgenden kurz auf die Studie von Suominen et al. eingegangen, die den
löslichen Transferrinrezeptor und den Ferritinindex als sensitive diagnostische Parameter für den
Eisenstatus von ansonsten gesunden Menschen herausstellen (Abb. 3) (11).
Abb. 6 Stadien des Eisenmangels und diagnostische Parameter nach Suominen et al. (11) Speichereisenmangel, 2.)
eisendefizitäre Erythropoese, 3. Eisenmangelanämie.
Dieses Konzept ist nicht sehr weit von dem alten Vorschlag von Heinrich und Hausmann entfernt und
ersetzt die älteren diagnostischen Parameter wie Serum-Eisen und Transferrin durch modernere
Parameter wie s-TfR und Ferritinindex.
Synthese der Konzepte
Es gibt zwei Arten von Patienten, bei denen der individuelle Eisenstatus wichtig für klinische
Entscheidungen ist.
Patienten mit „reinem“ Eisenmangel:
Für die allermeisten Patienten geht es um einen absoluten Eisenmangel, d.h. verschiedene
Kompartments werden bei fortlaufend negativer Eisenbilanz nacheinander bzw teilweise parallel entleert.
Hierfür ist die Einteilung von Hausmann und Heinrich aus dem Jahr 1972 immer noch ausreichend gut
geeignet. Jedes Labor kann Ferrin, Serum-Eisen und Transferrin messen, jede modernere, teuere
Methode ist schlicht unnötig. 
Stadium 1: Speichereisenmangel, bei dem die physiologischen Eisenreserven mobilisiert werden
und es zu vermehrten Transport aus den Speichern hin zu Geweben mit Eisenbedarf kommt. Das Serum-
Ferritin ist der beste Parameter für dieses Stadium, das evtl. bereits mit einer klinischen Symptomatik
verbunden sein kann. 
Stadium 2: Eisendefizitärer Stoffwechsel und Transport, ein Übergangszustand, bei dem der
Eisenbedarf in Geweben bereits defizitär wird. Das Knochenmark hat den höchsten Bedarf an Eisen und
wird sich bis zuletzt auf Kosten von anderen Geweben bedienen. Den idealen, umfassenden
diagnostischen Parameter für dieses Stadium gibt es. Die Beeinträchtigung des Transportpools im Blut ist
nach Heinrich und Hausmann leicht und einfach zu messen. Sie läuft sicher parallel mit einer
beginnenden eisendefizitären Erythropoese, angezeigt durch CHr <26-32 oder HYPO >10 %, oder ZPP,
oder sTfR. Diese eisendefizitäre Erythropese ist aber nur ein Teilaspekt dieses Stadiums.
Stadium 3: Eisenmangelanämie, das Stadium, in dem es auch für die Erythropoese gegenüber der Norm
nicht mehr reicht. Parallel wirken auch in anderen Geweben schwere Mangelzustände, die man
diagnostisch nicht so leicht verfolgen kann. 
Patienten mit chronischer Erkrankungen und/oder Therapie mit r-HuEPO:
Der Ausnahmepatient, bei dem der Eisenstoffwechsel durch die Grundkrankheit wesentlich beeinträchtigt
wird. Entzündungsreaktionen beeinflussen die Hepcidinsynthese und damit die wesentlichen
Eisentransportwege. Die durch r-HuEPO-Therapie angetriebene Erythropoese kann nicht schnell genug
mit Eisen aus den vorhandenen Eisenspeichern versorgt werden (=funktioneller Eisenmangel). Bei diesen
Patienten sind diagnostischen Parameter wie Serum-Ferritin und Transferrin-Fe-Sättigung wenig sensitiv
und spezifisch. Chr und HYPO sind besser geeignet als das flasch erhöhte Ferritin. Bei diesen Patienten
macht eine Stadieneinteilung eigentlich wenig Sinn, weil keine Aussage über mögliche Eisenspeicher
getroffen werden kann. Bei allen zur Verfügung stehenen „High-Tec-Parametern“ wird im Einzelfall doch
immer die Frage bestehen bleiben, ob der vorliegende Patient einen Eisenmangel hat oder nicht. Bei
Patienten mit renaler Anämie mit Ferritinwerten von 500-800 ng/ml wird ein funktioneller Test mit einer
begrenzten Eisentherapie als die endgültige Bestätigung für eine vorhandene Eisenmangelanämie
angesehen (z.B. 40 mg Fe-Sucrose bei jeder Dialyse über 8 Wochen) mit Testkriterium 1 g/dl Hb-Anstieg
in dieser Zeit (12). 
In der Praxis ist außerdem häufig nur die diagnostische Unterscheidung zwischen Eisenmangel mit und
ohne Anämie wichtig. Für Screeningstudien werden dabei „Cut-off-values“ wichtig, die mehr oder weniger
weltweit akzeptiert sind (Tabelle 1) 
Gruppe Hämoglobin (g/dL) Ferritin (µg/L) sTfR (mg/L) TfR/ log(Ferritin) Zn-PP µmol/mol Häm)
Prä-Menopausal 12,0 (13) <12-15 (13) >2.7 (15) >1.5 (16) >40 (17)
Schwangere 10,5 (2nd Trim) (14)
11,0 (1st, 3rd Trim) (14) <12-15 (13) > 4.4 > 2.2 >20 (18)
Männer und
postmeno-pausale Frauen 13,0 (13) <12-15 (13) >1.8 (15) >1.5 (15) >40 (17)
Tabelle 1: “Cut-off”-Werte von verschiedenen Eisenparametern für Eisen-mangelanämie sTfR, löslicher
Transferrinrezeptor, Zn-PP, Zink-Protoporphyrin.
Strittig ist vor allem der obere Ferritinwert, der die Normperson von einem Probanden mit
Speichereisenmangel unterscheidet. Wir halten nach Heinrich und Hausmann dafür einen Wert von < 35
ng/ml für den Übergang zu Eisenmangel, weil hier bereits die intestinale Eisenabsorption in vielen Fällen
bereits hochreguliert wird, was eine aktive Reaktion des Organismus auf einen „gespürten“
Spurenelementmangel aufzeigt. Bei einzelnen Probanden ist dies auch bei Ferritinwerten > 50 µg/l noch
der Fall. 
Literatur Einteilung
1.
Hausmann K, Kuse R, Meinecke KH, Bartels H, Heinrich HC. Diagnostic criteria of prelatent, latent and
manifest iron deficiency. Klin Wochenschr. 1971;49(21):1164-74.
2.
Cavill I, Macdougall IC. Functional iron deficiency. Blood, 1993; 82: 1377
3.
Macdougall IC, Hutton RD, Cavill I, Coles GA, Williams JD. Treating renal anaemia with recombinant
human erythropoietin: practical guidelines and a clinical algorithm. Br Med J 1990;300:655-9
4.
Wish JB. Assessing Iron Status: Beyond Serum Ferritin and Transferrin Saturation. Clin J Am Soc Nephrol
2006; 1: S4–S8,.
5.
Brugnara C, Chambers LA, Malynn E, Goldberg MA, Kruskall MS.Red blood cell regeneration induced by
subcutaneous recombinant erythropoietin: iron-deficient erythropoiesis in iron-replete subjects. Blood 1993;
15;81(4):956-64
6.
Goodnough LT. Erythropoietin and iron-restricted erythropoiesis Exp Hematol. 2007 35(4 Suppl 1):167-72
7.
Beguin Y, Grek V, Weber G, Sautois B, Paquot N, Pereira M, Scheen A, Lefebvre P, Fillet G. .Acute
functional iron deficiency in obese subjects during a very-low-energy all-protein diet13 Am J Clin Nutr
l997;66: 75-9.
8.
Swinkels DS, Wetzels JFM Hepcidin: a new tool in the management of anaemia in patients with chronic
kidney disease Department Nephrol Dial Transplant 2008; 23(8):2450-3.
9.
Hastka J, Lasserre JJ, Schwarzbeck A, Hehlmann R. Central role of zinc protoporphyrin in staging iron
deficiency. Clin Chem 1994;40:768–73
10.
Hastka J, Heimpel H, Metzgeroth G. Leitlinien Eisenmangel und Eisenmangelanämie (Oktober 2007) .
www.dgho.de
11.
Suominen P, Punnonen K, Rajamäki A, Irjala K. Serum Transferrin Receptor and Transferrin Receptor-
Ferritin Index Identify Healthy Subjects With Subclinical Iron Deficits Blood 1998; 92: 2934-2939
12.
Lin JL ,Chang MY, Tan DT, Leu ML. Short-Term Small-Dose Intravenous Iron Trial to Detect Functional
Iron Deficiency in Dialysis Patients. Am J Nephrol 2001;21:91–97
13.
WHO/NHD/01.3. Iron deficiency anemia assessment, prevention, and control. World Health Organization,
2001.
14.
Van der Broek N, Letsky E, White S, Shenkin A. Iron-deficient status in pregnant women: which
measurements are valid? Br J Haematol 1998; 103: 817-824
15.
Punnonen K., Irjala, K., Rajamaki, A. (1997) Serum transferrin receptor and its ratio to serum ferritin in the
diagnosis of iron deficiency. Blood 89:1052–1057
16.
Cook JD, Flowers CH, Skikne BS. The quantitative assessment of body iron. Blood 2003;101:3359-64
17.
Garrett S, Worwood M. Zinc protoporphyrin and iron deficient erythropoiesis. Acta Haematol 1994;
91:21–25.
18.
Van der Broek N, Letsky E, White S, Shenkin A. Iron-deficient status in pregnant women: which
measurements are valid? Br J Haematol 1998; 103: 817-824

Obwohl entsprechende diagnostische Kriterien seit
Jahrzehnten bekannt sind, gibt es bis heute keine weltweit
akzeptierte Einteilung für Eisenmangel. Im Folgenden
werden die gängigsten Konzepte vorgestellt. 
Prälatenter, latenter und manifester Eisenmangel 
Eine schlüssige und praxisbewährte rein diagnostische
Einteilung stammt von Hausmann und Heinrich aus den
70-ziger Jahren (1). Dabei wurden die klassischen
Blutparameter (Serum Ferritin, Hämoglobin, Serum Eisen,
Transferrin) mit aufwendigeren Techniken wie
histochemische Beurteilung von Eisen in
Knochenmarksausstrichen, der 59Fe-Absorption,
erschöpfende Phlebotomien an 425 Patienten verglichen.
Die Hochregulation der intestinalen Eisenabsorption
beginnt bereits bei der Entleerung der Eisenspeicher, was
zuverlässig am Absinken des Serum-Ferritins bei
normalem Hämoglobin erkannt werden kann. Dieses
Stadium wird als prälatenter Eisenmangel bezeichnet
(Abb. 1)